

Abbreviation (ISO4): Chinese Journal of Alzheimer's Disease and Related Disorders
Editor in chief: Jun WANG
Chinese Journal of Alzheimer's Disease and Related Disorders >
A study of social novelty of an Alzheimer's disease model
Received date: 2021-08-22
Revised date: 2021-09-15
Online published: 2021-12-25
Objective: To explore the social novelty of 5×FAD transgenic mice, and to provide a theoretical basis for the rational application of 5×FAD mouse model to study AD-related behaviors. Methods: Aβ pathology of wild-type mice and 5×FAD mice was examined by immunohistochemical staining; Three chambers tests were carried out to evaluate wild-type and 5×FAD mice aged at 4-5 months. The interaction time between wild-type and 5×FAD mice with S2 mice, the total distance and time in the novelty exploration stage of three chamber tests were recorded. GraphPad Prism 5.0 software, unpaired-t test was performed for statistical analysis. Results: a large number of Aβ plaques were distributed in the cerebral cortex of 5×FAD mice; The average interaction time between wild-type and S1/2 was (95.5 ± 27.22/ 264.6 ± 58.38) s, P < 0.05. The average interaction time between 5×FAD mice and S 1/2 was (91.02 ± 19.49/ 230.2±60.18) s, P < 0.05. There was no difference in interaction time between wild-type and 5×FAD mice with S2, P > 0.05. The total distance of wild-type mice and 5×FAD mice during the tests was (10710 ± 1781/ 9017 ± 1402) mm respectively, P > 0.05. The average speed of wild-type and 5×FAD mice in the equipment was (47.7 ± 5.453/ 37.24 ± 4.590) mm/s respectively, P > 0.05. Conclusion: 5×FAD mice displayed severe Aβ plaques pathology at the age of 5 months, and their social novelty behavior is no different from that of wild-type mice.
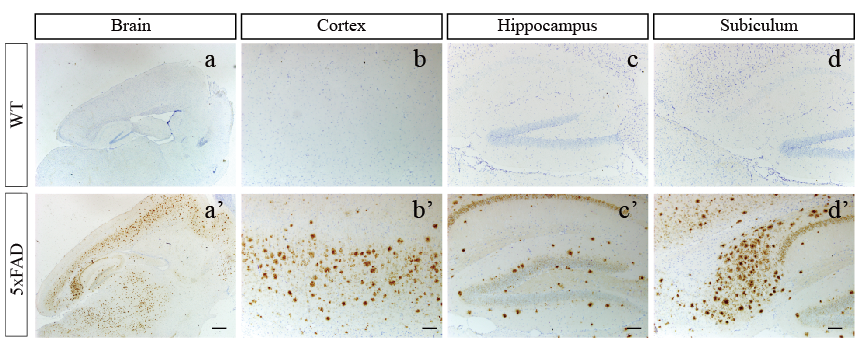
Key words: Alzheimer's disease; transgenic mice; Aβ plaque; social novelty
YE Xiao-lian , TAI Guang-ping . A study of social novelty of an Alzheimer's disease model[J]. Chinese Journal of Alzheimer's Disease and Related Disorders, 2021 , 4(4) : 310 -313 . DOI: 10.3969/j.issn.2096-5516.2021.04.011
| [1] |
Alzheimer's Association. 2015 Alzheimer's disease facts and figures[J]. Alzheimer's & dementia : the journal of the Alzheimer's Association, 2015, 11(3): 332-384.
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
/
| 〈 |
|
〉 |