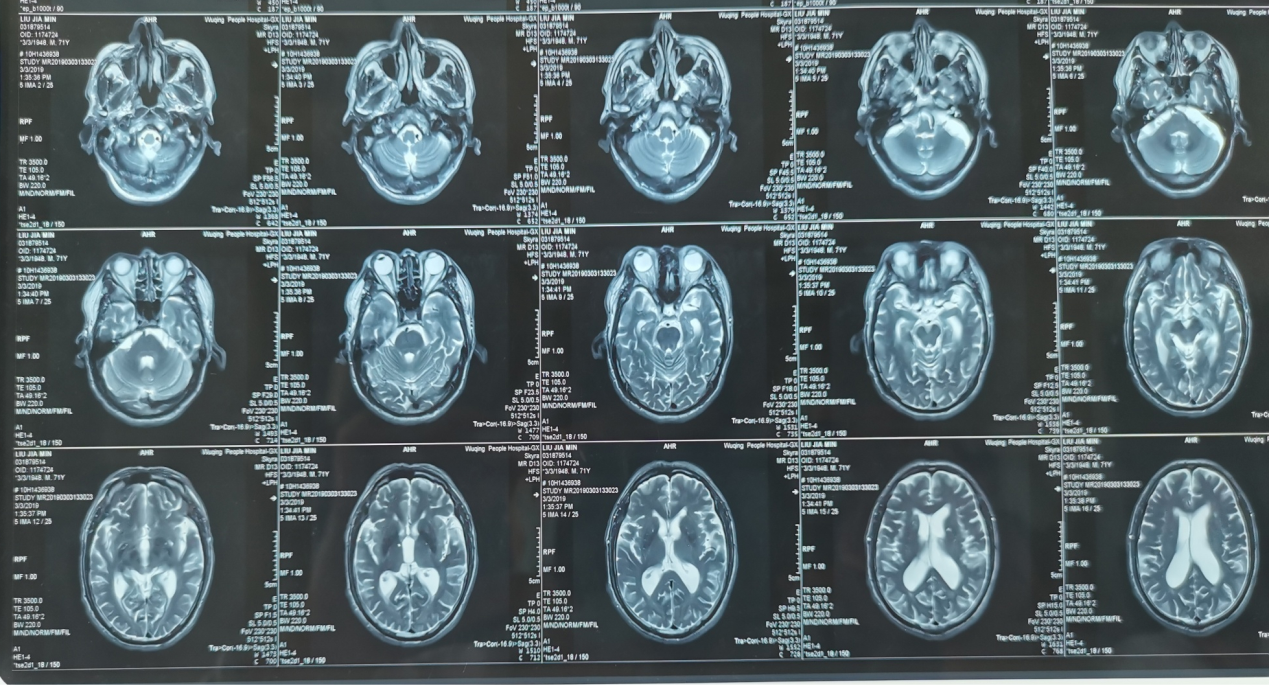
该患者记忆力下降、行动迟缓进行性加重,且存在快速进展、难以控制的四肢震颤,拟行立体定向脑深部电刺激器植入术(deep brain stimulator, DBS),需要首先考虑患者的诊断问题。该患者隐匿起病,进行性痴呆,存在多个认知域的损害,无明显精神行为异常,无幻觉,无明显的症状波动,依据2019年修订的NINCDS-ADRDA标准,首先考虑阿尔茨海默病(Alzheimer's disease, AD)。该患者存在诊断AD的核心症状:记忆障碍,MMSE评分7分,生活能力下降,ADL20分(满分100分);存在如下支持症状:MRI提示内颞叶萎缩,MTA=3;PET/CT提示双侧颞叶糖代谢减,符合AD的诊断标准。但患者诊断AD,需把如下两个问题解释清楚:其一,就AD而言,症状进展过于快速。众所周知,AD是认知障碍中最常见的一种,全世界AD的患病率在4000万人以上。一般来说,其病程缓慢进展
[1]。然而,随着对AD研究的深入,越来越多的证据表明临床表型和进展率存在变异性
[2⇓-4],因此提出了快速进展型AD (rapidly progressive form of AD, rpAD)的概念。rpAD的临床定义各研究不尽相同:①MMSE评分年下降5分以上
[5,6]或②半年内MMSE下降4分以上
[3]可以诊断rpAD。有研究认为造成rpAD的原因与APOE基因的不同多态性以及淀粉样蛋白ß42的不同构象特征有关
[4]。该患者1年内MMSE评分从19分下降到12分,MMSE评分年下降7分(>5分)符合rpAD的诊断标椎,所以我们考虑该患者有rpAD的可能。其二,如何解释该患者合并的锥体外系症状?有研究认为锥体外系症状,如强直、迟缓、姿势障碍是AD患者常见的临床特征。AD患者锥体外系症状的患病率在轻度阶段约为12%,到疾病晚期达92%,以运动迟缓和僵硬常见。65岁以上发病的患者可以同时表现出AD和PD的临床特征。18%~85%的尸检确诊的AD患者发生了伴有路易小体形成的黑质变性,提示AD与PD同时存在的病理机制
[9]。锥体外系症状的存在并不一定意味着PD的存在。在一些存在锥体外系症状且尸检证实的散发性AD患者中,并未发现路易小体,甚至黑质结构没有任何异常,包括路易小体的形成,其发生锥体外系症状的机制尚不清楚,其可能原因:有锥体外系症状的AD患者黑质的神经原纤维缠结比无锥体外系症状的AD患者多。那么,该患者是否合并PD呢?该患者有帕金森综合征的症状及体征
[10],多巴胺能药物治疗具有明确且显著的有效应答,支持PD的诊断,但该患者存在明确诊断PD的警示征象:在发病5年内出现快速进展的步态障碍,需要规律使用轮椅,不符合典型PD的诊断标椎。近年有学者提出了非典型帕金森氏病的概念
[9],快速进展也是其诊断标准之一。该患者虽然PET/CT提示双侧额叶、颞顶联合区及颞叶皮层局限性片状放射性分布减低,考虑神经变性型痴呆(AD可能),但因为种种原因未能行多巴胺转运体PET/CT检查,亦未能行PD相关基因检测,其锥体外系症状尚不能除外PD的可能。所以,我们认为该患者诊断考虑快速进展的AD合并非典型帕金森氏病的可能性更大。该患者存在认知障碍,影像上提示脑室系统扩大,腰穿放液试验(-),可以除外合并正常颅压脑积水的可能。