

Abbreviation (ISO4): Chinese Journal of Alzheimer's Disease and Related Disorders
Editor in chief: Jun WANG
Chinese Journal of Alzheimer's Disease and Related Disorders >
Progressive supranuclear palsy with mimic normal pressure hydrocephalus: A case report and research progress
Received date: 2021-01-15
Revised date: 2021-03-02
Online published: 2021-06-25
Objective: To demonstrate a PSP patient which appeared iNPH-like magnetic resonance imaging (MRI) features. Methods: Analyze the diagnosis and treatment of a PSP patient in our hospital, and review the relevant research progress. Results: This patient presented with dyskinesia, stiff limbs, cognitive impairment, dysphagia and dyslalia; The MRI features conclude midbrain atrophy and signal changes.Midbrain atrophy presents “morning glory sign” in axial plane and “hummingbird sign” (HBS)in the median sagittal plane. The third and fourth ventricles were enlarged, the Evan's index>0.34. Cerebrospinal fluid (CSF) tap/shunt treatment in this case resulted in short-term benefits but subsequent deterioration ensued within one year. And the effect of large doses of dopa serazine was not good. Conclusion: This study demonstrated that some PSP patients develop iNPH-like MRI features, suggesting the presence of iNPH-like features in clinical spectrum of PSP. An awareness that PSP can mimic the clinical symptoms of iNPH may help to avoid invasive cerebrospinal fluid shunting procedures.
LIU Ying , YANG Fu-xia , GU Chun-hui , WEI Wen-shi . Progressive supranuclear palsy with mimic normal pressure hydrocephalus: A case report and research progress[J]. Chinese Journal of Alzheimer's Disease and Related Disorders, 2021 , 4(2) : 134 -137 . DOI: 10.3969/j.issn.2096-5516.2021.02.010
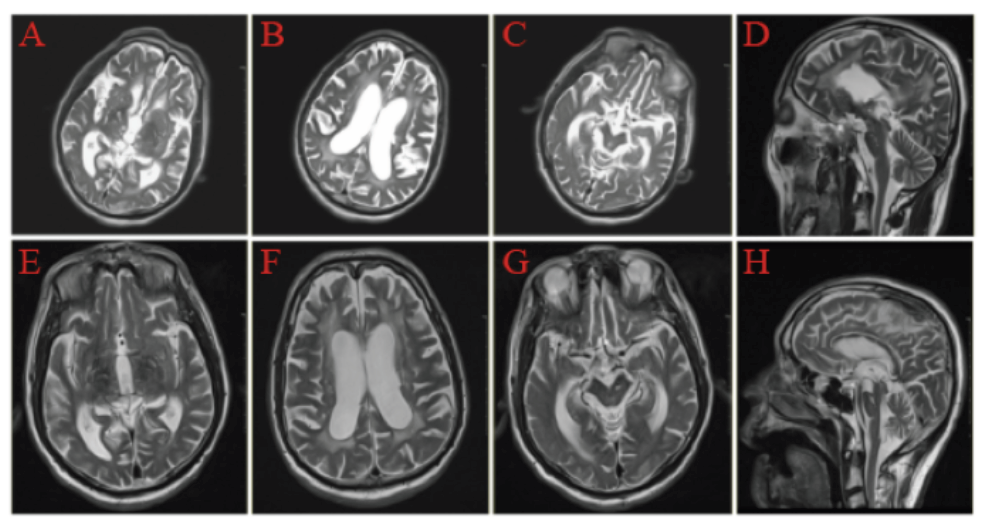
图1 患者疾病不同时期的MRI特征A-D为患者2018年头颅MRI,E-H为患者2021年头颅MRI。A和E头颅MRI示第三脑室扩大,外侧裂增宽;B和F头颅MRI示侧脑室扩大,双侧额颞叶萎缩;C和G头颅MRI冠状位示中脑前后径变小,导水管扩张,呈“牵牛花征”;D头颅MRI矢状位可见中脑萎缩,H头颅MRI矢状位见中脑被盖部平坦,呈“蜂鸟征”。 Fig. 1 The typical MRI imaging of a patient at different periods A-D:The patient's head MRI in 2018,E-H:The patient's head MRI in 2021. The head MRI in figure A and E showed enlargement of the third ventricle and widen of sylvian fissure; The head MRI in figure B and F showed enlargement of lateral ventricles and atrophy of bilateral frontotemporal lobes; The head MRI in figure C and G showed reduction of anterior and posterior diameter of the midbrain and expansion of mesencephalic aqueduct, presented the "morning glory sign"; the head MRI sagittal plane in figure D showed midbrain atrophy, the head MRI sagittal plane in figure H showed the midbrain cover was flat, showing "hummingbird sign". |
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
/
| 〈 |
|
〉 |